Медицинская химия (Medicinal chemistry). Мед химия
Медицинская химия, введение. (Лекция 1)
1. Лекция 1 Медицинская химия, введение. История возникновения, предмет дисциплины. Задачи медицинской химии. Связь с современными технология
Лекция 1 Медицинская химия, введение. История возникновения, предмет дисциплины. Задачи медицинской химии. Связь с современными технологиями разработки лекарств К.В. Балакин Каф. общей химии МФТИ2. Информация о лекторе Константин Валерьевич Балакин
Образование 1993 – Московский институт тонкой химической технологии, специальности – биотехнология, тонкий органический синтез; 1993-1996 – аспирантура ИБХ РАН; 1998 – степень кандидата химических наук, специальность биоорганическая химия 2005 – доктор химических наук, специальность органическая химия (ИГХТУ, Иваново). Профессиональная деятельность 2000-2008 – руководитель отделов научного маркетинга и медицинской химии, ЦВТ ХимРар. 2008-2012 – зав. лабораторией в ИФАВ РАН (Черноголовка). 2008 по н.в. – директор некоммерческого партнерства институтов РАН «Орхимед» (Москва). 2012 по н.в. – зав. кафедрой общей химии МФТИ (ГУ) (Долгопрудный). 2014 по н.в. – директор Калужского фармкластера Автор более 100 научных публикаций в области органической и медицинской химии. Сферы деятельности - Научная и образовательная сфера - Индустрия разработки лекарств - Экспертиза фармацевтических и биомедицинских технологий3. Медицинская химия. История возникновения. Предмет дисциплины
Зефирова О.Н., Зефиров Н.С. Вестник Моск. Унив. 2000.5. История
Даты Открытия Авторы XVI в. до н.э. Первое из известных описаний лекарственных средств в Египте (упоминаются опий, гиосциламус, слабительное из растения клещевина, мята, бальзамы, печень и др.) Папирус Эберса (автор неизвестен) IV-III в. до н.э. Систематизация показаний к применению лекарственных средств древней медицины. Гиппократ I в. н.э. Описание более 900 лекарственных средств (применяемых) Диоскорид II в. н.э. Разработка принципов лечебного и профилактического назначения лекарственных средств. Первые шаги к очистки лекарственных средств от балластных элементов. Гален X-XI в. Систематизация лекарственных средств и показаний к их применению. Абу-Али Ибн Сина (Авиценна) XV-XVI в. Внедрение в практическую медицину солей металлов (ртуть — для лечения сифилиса) Парацельс 1800-1850 гг. Выделения из опия алкалоиды морфина. Внедрение экспериментов на животных в фармакологию. Анализ действия стрихнина. Выделение из коры хинного дерева алкалоида хинина. Выделение алкалоида атропина. Применение для хирургического наркоза азота закиси. Первая демонстрация наркотического действия эфира. Применение для хирургического наркоза хлороформа. Выделение из опия алкалоиды папаверина. Установление механизма действия Кураре Сертюрнер, Мажанди, Пеллетье, Кавенту, Майн и др. 1850-1900 гг. Внедрение в практику снотворного средства хлоргидрата. Применение нитроглицерина для лечения «грудной жабы». Открытие анестезирующих свойств у кокаина Либрих, Меррил, Анреп. 1900-1925 гг. Получение синтетического анестетика новокаина. Разработка общих принципов химиотерапии. Получение и применение противоспирохетозного средства сальварсана. Выделение первого витамина (В1). Выделение гепарина Эйнхорн, Эрлих, Функ, Мак-Лен, Хауэл 1925 –1950 гг. Выделение инсулина. Открытие пенициллина Открытие противогистаминных средств. Выделение и применение в медицинской практике кортизона. Выделение противотуберкулезного средства стрептомицина Бентинг, Бест, Флеминг, Бовэ, Кэндал, Райхштейш, Хенч, Ваксман 1950-1975 гг. Получение и применение в медицинской практике первого нейтролептика — аминазина. Внедрение в практику первого противодиабетического средства из группы производных сульфонилмочевины, эффективного при приеме внутрь. Получение симпатолика гуанетидина (октадина). Получение первого блокатора a-адренорецепторов. Синтез инсулина. Получение блокаторов Н2-гистаминорецепторов. Выделение эндогенных болеутоляющих веществ — энкефалинов и эндорфинов Шарпантье, Курвуазье, Лаборн, Франке, Фукс, Мелл, Максвелл, Пауэлл, Слэтер, Катсоянис, Юлэк, Хьюз, Костерлиц, Ерениус, Ли6. История медицинской химии
Примеры из Зефирова О.Н., Зефиров Н.С. Вестник Моск. Унив. 2000.7. История медицинской химии
1950-60 гг., транквилизаторы, антидепрессанты Примеры из Зефирова О.Н., Зефиров Н.С. Вестник Моск. Унив. 2000.8. История медицинской химии
1950-60 гг., Лекарства для лечения сердечно-сосудистых заболеваний Примеры из Зефирова О.Н., Зефиров Н.С. Вестник Моск. Унив. 2000.9. Фармакология в России
Даты Открытия Авторы 30-е годы XIX века Использование белильной извести в качестве дезинфицирующего средства Нелюбин 1847 г. Широкое использование эфира в военно-полевой хирургии Пирогов 1865 г. Установление специфического действия препаратов строфанта на сердце Пеликан 1900 -1901 гг. Сформулированы принципы получения инсулина Соболев 1909 г. Получение и применение в хирургии гедонала- первого средства для внутривенного наркоза Кравков, Федеоров 1910 — 1936 гг. Изучение влияния веществ (бромидов и др.) на высшую нервную деятельность Павлов 1928г. Установление принципа действия сердечных гликозидов при сердечной недостаточности Аничков, Тренделенбург 30-е годы XX века Разработка синаптической теории действия веществ на центральную нервную систему Закусов 30-е-70-е годы XX века Исследования избирательности действия медиаторных средств Аничков 1942 г. Получение пенициллина в СССР Ермолаева 1956 — 1958 гг. Получение противобластомных средств саркомицина и допана Ларионов10. Медицинская химия в России
Акад. Н.С. Зефиров и сотр. (МГУ им. Ломоносова) Акад. А.И. Арчаков и сотр. (НИИ БМХ им. Ореховича, Москва) Член-корр. РАН С.О. Бачурин и сотр. (ИФАВ РАН, Черноголовка) Акад. Г.А. Толстиков (Новосибирск) Акад. М.С. Юнусов (Уфа) Акад. О.Г. Синяшин (Казань) Акад. М.П. Егоров и Ю.Н. Бубнов (ИОХ и ИНЭОС, Москва) Член-корр. РАН А.В. Кучин (ИХ РАН, Сыктывкар) и многие другие11. Предмет медицинской химии
«Предметом медицинской химии является открытие, разработка и идентификация биологически активных соединений, а также интерпретация механизма их действия на молекулярном уровне. Основной акцент делается на лекарства, но интересы медицинской химии не ограничиваются лекарствами, а включают биологически активные соединения вообще. Предметом медицинской химии является также изучение, идентификация и синтез продуктов метаболизма этих лекарств и родственных соединений» IUPAC, 1996. Медицинская химия – наука междисциплинарная, на границе (с пересечением) органической химии, биохимии, биоорганической химии, фармакологии и фармацевтической химии.12. Медицинская химия - Фармакология
Фармакология [от греческого Pharmakon (лекарство) и Logos (учение, слово)] – наука о взаимодействии лекарственных веществ с организмом и о путях изыскания новых лекарственных средств [Краткая медицинская энциклопедия. Т. 3. М., 1990. С. 288]. Есть и более короткое определение: «Фармакология – наука о лекарствах». Фармакология и ее раздел, фармацевтическая химия, не дают ответа на ключевой вопрос: какую структуру надо синтезировать, чтобы создать лекарственное соединение. Именно этот вопрос занимает в медицинской химии центральное место!13. Другая «медицинская химия»
Сравните: англ. Medicinal chemistry – рус. Медицинская химия англ. Medical chemistry – рус. Медицинская химия Медицинская химия (medical chemistry) - это, в сущности, «биохимия патологических состояний». Одним из основных предметов ее исследований является разработка различных аналитических методов, используемых в диагностических целях, и поэтому ее можно считать разделом медицины. В рамках настоящего курса мы изучаем медицинскую химию (medicinal chemistry)!14. Медицинская химия
Медицинская химия (medicinal chemistry, chimie therapeutique, Arzneimittelforschung) – это наука, не являющаяся разделом биологии или медицины, а являющаяся в первую очередь специфическим разделом органической химии на стыке с биохимией, биоорганической химией и фармакологией, а в последние годы – и математическими дисциплинами. Медицинская химия имеет свою собственную систему понятий и определений, а также специфический инструментарий, что делает ее самостоятельной дисциплиной. Медицинская химия играет роль своеобразного переводчика биохимической информации на язык структурных формул.15. Пример
Медицинская (химиотерапевтическая) задача: создание препарата для лечения язвы желудка. 1) одним из факторов, способствующих возникновению и развитию ЯЖ, является повышенное выделение соляной кислоты. В случае тяжелых форм заболевания (частые повторные кровотечения, значительное кислотообразование и т.д.) обычная терапия (использование антацидных препаратов, например, гидроокиси алюминия и др.) часто оказывается неэффективной; 2) выделение желудочного сока регулирует эндогенный медиатор – гистамин – посредством связывания с Н2-рецептором. Уменьшить выделение кислоты можно созданием специфического антагониста Н2рецептора, блокирующего его действие. Задача оказывается неразрешимой для химика-органика, поскольку очевидно выходит за рамки этой дисциплины Пример из Зефирова О.Н., Зефиров Н.С. Вестник Моск. Унив. 2000.16. Пример
Медицинская (химиотерапевтическая) задача: создание препарата для лечения язвы желудка. Инструментарий медицинского химика: - Поиск в специализированных базах данных ингибиторов гистаминовых рецепторов. - Дизайн биоизостерных аналогов имеющихся активных соединений. - Создание фармакофорных гипотез и соответствующих химических структур. - Молекулярный докинг. - Специальные методы анализа данных, направленные на создание Н2специфичных соединений. - Дизайн, основанный на методах молекулярного подобия. - Хемогеномика, и т.д. и т.п.17. Аспекты взаимодействия лекарства и организма. Задачи медицинской химии
18. Человек и лекарство аспекты взаимодействия
O O S O N H O N19. Молекулярная биомишень
Биомишень (biotarget) – в организме человека Биомишень – в организме патогенного организма (бактерия, вирус) Природа биомишени (белок, ДНК, клеточные стенки, субклеточные структуры, напр., митохондрии, и пр.) Вид белковой биомишени (рецепторы, ферменты) Взаимодействие с другими биомишенями (мультитаргетность) Задачи для медицинского химика: Дизайн химических соединений, направленный на поиск соединений, обладающих определенным профилем мишень-специфической активности.20. Способ введения (administration route)
• Энтеральные (через желудочнокишечный тракт) Пероральное, сублингвальное, ректальное • Парентеральные (минуя ЖКТ) Инъекции (подкожные, внутримышечные, внутривенные, внутриартериальные, другие), ингаляции, трансдермальные Задачи для медицинского химика: Дизайн химических соединений, направленный на увеличение эффективности проникновения через биомембраны (ЖКТ, ГЭБ, кожа, плацента и др.), улучшение растворимости, оптимизацию метаболитического профиля и др.21. Лекарственная форма
• твердые таблетки, порошки, капсулы • жидкие стерильные (для инъекций), нестерильные (капли, накожные аппликации и пр.) • газообразные ингаляционные Задачи для медицинского химика: Дизайн химических соединений, направленный на оптимизацию свойств готовой лекарственной формы (ГЛФ), улучшение растворимости, термодинамической стабильности твердых форм, метаболитической стабильности и пр.22. Безопасность
• токсичность острая, субхроническая, хроническая, специфическая • токсичность для окружающей среды • лекарство-лекарственные взаимодействия (drug-drug interactions) по механизму ингибирования цитохромов Р450, по другим механизмам • взаимодействие со специфическими биомишенями Например, ингибирование белка hERG вызывает кардиотоксичность Задачи для медицинского химика: Дизайн химических соединений, направленный на снижение токсичности, оптимизацию профиля взаимодействия с цитохромами Р450 и другими метаболизирующими ферментами, взаимодействия со специфическими биомишенями23. ADME параметры
Absorption, Distribution, Metabolism, Excretion • Более 40% активных субстанций не проходят (до)клинические испытания по причине неоптимальных ADME-свойств • Существуют многочисленные экспериментальные способы оценки, но они очень дороги, особенно для больших библиотек соединений • Компьютерные методы приближаются по точности к экспериментальным Задачи для медицинского химика: Дизайн химических соединений, направленный на оптимизацию проникновения через ЖКТ и ГЭБ; метаболитической стабильности; фармакокинетических параметров – время полужизни в плазме, объем распределения, связывание с белками плазмы; распределение в органах и тканях и др.24. Связь медицинской химии с современными технологиями разработки лекарств
25. Разработка лекарств классическая схема
Синтез веществ, выделение из природных источников Биологические испытания (доклинические, клинические) лекарство Традиционный подход: десятки соединений испытываются на нескольких моделях (изначально – непосредственно на человеке). Активные вещества становятся лекарствами.26. Разработка лекарств современная схема
Виртуальный скрининг библиотек соединений Синтез веществ, выделение из природных источников Высокопроизво дительный скрининг на биомишени Поиск биомишеней, разработка метода тестирования лекарство Современный подход: миллионы соединений в виртуальных библиотеках, сотни тысяч – в ВПС, десятки в in vivo исследованиях, единицы – в клинических. Биологические испытания (доклинические) Биологические испытания (клинические)27. Разработка лекарств триада методов
Виртуальный скрининг библиотек соединений «Лидер» («лид») lead Синтез веществ, выделение из природных источников Хит-ту-лид оптимизация: компьютерный дизайн, ресинтез, биотестирование Высокопроизво дительный скрининг на биомишенях Оптимизированный «хит» hit Процесс итеративный, предполагает последовательные циклы компьютерного отбора, (ре)синтеза, скрининга28. Виртуальный скрининг (ВС)
Совокупность компьютерных методов, обычно высокопроизводительных, позволяющих идентифицировать соединения (группы соединений) в больших виртуальных библиотеках химических структур, которые обладают повышенной вероятностью проявления заданных фармакологических свойств29. Комбинаторный синтез
Zimmermann, Robert Langer & Daniel G Anderson Nature Biotechnology 26, 561 - 569 (2008) N = 17 * 117 = 198930. Комбинаторный взрыв
Одна библиотека: 5 точек рандомизации, 100 реагентов с отдельными функциями, N = 1005 = 10 млрд соединений Реагентов отдельного вида могут быть тысячи (R-COOH, RR’NH, RSO2Cl, RCOCH=Ch3, RCh3Cl и т.д.) Реально синтезируют не более 500 соединений на одну библиотеку (ХимРар). Как отобрать эти соединения? Нужны методы рационального отбора или направленного дизайна!31. Основа ВПБС – действие на биомишень
32. Биомишени
33. Биомишени для лекарств
Ионные каналы Рецепторы сопряженные с G-белками Ядерные рецепторы Ферментные системы клеток В настоящее время известно около 500 биомишеней. Потенциально – 5-10 тыс. биомишеней34. Высокопроизводительный скрининг
• Наиболее производительные системы ВПС могут скринировать до 1 млн. образцов в день. • Лимитирующей стадией становится анализ результатов ВПС.35. Экономика
Время постройки пирамиды – 12-15 лет, цена пирамиды – до 1 млрд. долларов 1 рынок 2-3 клиника 5-6 доклиника 10-12 лидеров 400-500 хитов 100 000 соединений Очевидный ресурс – улучшение методов рационального дизайна и отбора соединений для синтеза и скрининга на основе современных медицинско-химических концепций36. Место медицинской химии
• Виртуальный скрининг Рациональный отбор соединений на основе медицинскохимических концепций • Комбинаторный синтез Дизайн и оптимизация комбинаторных библиотек с использованием медицинско-химических концепций • Биологический скрининг «Хит-ту-лид» оптимизация с применением медицинско-химического инструментария37. Благодарю за внимание! E-mail: [email protected]
ppt-online.org
Медицинская химия (Medicinal chemistry) | marinky
О проекте
Новый проект "Медицинская химия" – статьи про медицинскую химию, разработку лекарств и применение в ней компьютерных технологий, фармакологию, сопровождающиеся красочными иллюстрациями и видео. В подготовке материала используются различные источники. Проект в стадии активной разработки:) В целях популяризации науки…
Постеры
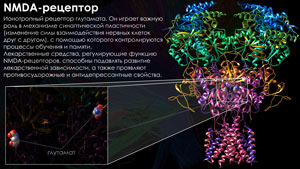 NMDA рецептор
NMDA рецептор
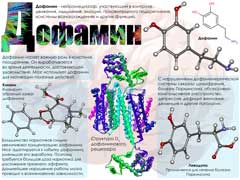 Дофамин
Дофамин
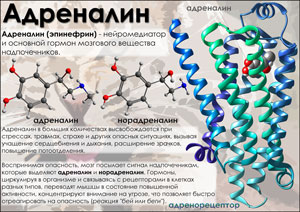 Адреналин
Адреналин
 Гемоглобин
Гемоглобин
Материалы раздела «Медицинская химия» – статьи, модели молекул, тезисы…

CDK4 — циклинзависимая киназа 4
Модели молекул циклинзависимой киназы 4 (CDK4) — картинки и анимации.Циклинзависимая киназа 4 — регулируемый циклином белок, играющий ключевую роль в регуляции клеточного цикла. Важная терапевтическая мишень.
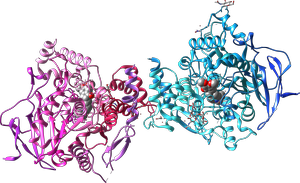
Ацетилхолинэстераза
Модели молекул ацетилхолинэстеразы и её ингибитора донепезила — картинки и анимации.…Для передачи нового сигнала необходимо удалить «отработавший» ацетилхолин из синаптической щели. Ацетилхолинэстераза катализирует гидролиз ацетилхолина до холина и уксусной кислоты…

Молекулярное моделирование
Различные изображения, анимации и видео на тему молекулярного моделирования и разработки лекарств: симуляция взаимодействия лекарства с терапевтической мишенью, модели молекул лекарственных препаратов и рецепторов.

Докинг
Статья носит популяризационный характер и отражает мое (возможно не совсем корректное) понимание докинга на основе прочитанной литературы и пользования прикладными программами. Когда это самое "понимание" изменится, я обязательно напишу еще одну статью 🙂
Описаны основные принципы молекулярного докинга, алгоритмы и процесс докинга, виртуальный скрининг…
Свойства ведущих соединений
Рассмотрены такие свойства ведущих соединений (лидеров), как биологическая доступность, растворимость, структура, устойчивость. Статья сопроваждается 2D и 3D моделями молекул лекарств (картинки и анимации) и видео взаимодействия лекарства с мишенью.
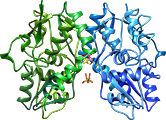
Участки связывания рацетамов с AMPA-рецепторами
Общая характеристика рацетамов, новые участки связывания пирацетама и анирацетама с AMPA-рецепторами. 3D модели молекул пирацетама, анирацетама, ГАМК, изображения участков связывания, видео докинга.

Тезисы Molecular Modeling – A Modern Approach to Drug Discovery
Тезисы к докладу на конференции по химии на английском языке. Молекулярное моделирование – современный подход к разработке лекарств. Принципы молекулярного моделирования. Разработка лекарств. Применение молекулярного моделирования.
Rational drug discovery is one of the most actual issues of medicinal chemistry. Application of molecular modelling techniques can bring discovery of drugs to new level with minimal costs…
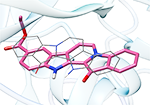
Тезисы MOLECULAR DOCKING STUDY OF FASCAPLYSIN DERIVATIVES INTERACTION WITH CDK4
Fascaplysin is a red pigment that was isolated in 1988 from marine sponge Fascaplysinopsis sp. This alkaloid exhibits antifungal, antibacterial, antiviral properties and anticancer activity against a wide range of tumor cells. Fascaplysin is a highly selective inhibitor of cyclin-dependent kinase 4 (CDK4) which plays a key role in cell cycle regulation and is an important target for anticancer drugs.
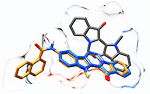
Тезисы FASCAPLYSIN DERIVATIVES AS μ-OPIOID RECEPTOR AGONISTS: MOLECULAR MODELING STUDY
Fascaplysin is a sponge-derived red pigment that exhibits a wide range of biological activity among which are antibacterial, antifungal, antiviral and anticancer properties. Recently it was reported that fascaplysin serves as selective μ–opioid receptor (MOR) agonist with a signaling profile that resembles endorphins. It makes fascaplysin a perspective compound for development of novel analgesics with reduced side effects.
- Protein Data Bank – трехмерные структуры макромолекул
- Chemspider – 2D и 3D структуры химических соединений
- Кафедра медицинской химии и тонкого органического синтеза МГУ
- UCSF Chimera—a visualization system for exploratory research and analysis. Pettersen EF, Goddard TD, Huang CC, Couch GS, Greenblatt DM, Meng EC, Ferrin TE. J Comput Chem. 2004 Oct;25(13):1605-12.
- O. Trott, A. J. Olson, AutoDock Vina: improving the speed and accuracy of docking with a new scoring function, efficient optimization and multithreading, Journal of Computational Chemistry 31 (2010) 455-461
- Morris, G. M., Huey, R., Lindstrom, W., Sanner, M. F., Belew, R. K., Goodsell, D. S. and Olson, A. J. (2009) Autodock4 and AutoDockTools4: automated docking with selective receptor flexiblity. J. Computational Chemistry 2009, 16: 2785-91.
- Thomas G. Medicinal Chemistry. Chichester: John Wiley; 2007.
- Nadendla R. Principals Of Organic Medicinal Chemistry. New Delhi: New Age International; 2005.
- Patrick G. An Introduction To Medicinal Chemistry. Oxford: Oxford University Press; 2005.
marinky.com
Химия и медицина
Илья Абрамович Леенсон«Химия и жизнь» №4, 2011
Первые успехи

Одно из самых заметных достижений органического синтеза ХХ столетия — получение новых лекарственных средств. В результате многие болезни, которые раньше считались смертельными, перешли в разряд излечимых. В VI веке чума уничтожила половину населения Византийской империи, а в XIV веке только за три года — с 1347 по 1350-й — в Европе от чумы умерло 25 миллионов человек. Миллионами исчисляются жертвы гриппа 1918 года («испанки»). Синтез в лабораториях новых лекарственных средств и их последующее внедрение в медицинскую практику, вероятно, спасли от смерти на протяжении ХХ века сотни миллионов человеческих жизней.
Во второй половине XIX века быстрыми темпами начала развиваться синтетическая органическая химия. Она дала людям красители, душистые вещества, лекарственные средства. Тем не менее еще в начале ХХ века число индивидуальных химических соединений, применявшихся в качестве лекарственных средств, исчислялось единицами. Начало химиотерапии — лечению болезней с применением химических препаратов — положил немецкий врач, бактериолог и биохимик Пауль Эрлих. В 1891 году он предложил применить для лечения малярии краситель метиленовый синий. Однако это соединение не могло конкурировать с природным хинином. Позже Эрлих прославился сальварсаном, «волшебной пулей», первым эффективным средством против сифилиса.
Между синтезом нового соединения и его применением в медицине иногда проходили десятилетия. С XIX века была известна сульфаниловая (п-аминобензолсульфоновая) кислота h3N—C6h5—SO3H. Впервые ее получил еще в 1845 году французский химик Шарль Фредерик Жерар. В 1908 году был получен амид этой кислоты h3N—C6h5—SO2—Nh3, а затем и его N-замещенные (по амидной группе) производные с общей формулой h3N—C6h5—SO2—NH—R, которые получили название сульфаниламидов. Но только 27 лет спустя немецкий химик Герхард Домагк выяснил, что соединения этой группы убивают многие микроорганизмы и их можно использовать для лечения ряда инфекционных заболеваний.
Первым синтетическим лечебным препаратом был азокраситель красного цвета пронтозил (красный стрептоцид) h3N—C6h5—N=N—C6h5—SO2—Nh3, который синтезировали в 1932 году немецкие химики Фриц Митч и Йозеф Кларер. Домагк исследовал действие этого препарата на множестве мышей, получивших десятикратную смертельную дозу культуры гемолитического стрептококка. Эффект был поразительным: все мыши остались живы, тогда как в контрольной группе все погибли. Это было первое в мире лекарственное средство, давшее такие прекрасные результаты. Необходимо было провести испытание на людях. Именно в это время маленькая дочь Домагка уколола себе палец. В ранку попала инфекция, образовался нарыв, и началось заражение крови. В больнице хирурги очистили нарыв, но заражение не проходило, положение становилось угрожающим. И Домагк решился испытать на дочери пронтозил. Результат не заставил себя ждать: нарыв прошел, девочка выздоровела. Средство помогало также при воспалении легких, при некоторых других болезнях. В 1939 году Домагку за открытие первого антибактериального препарата была присуждена Нобелевская премия по физиологии и медицине.
В конце 1935 года было показано: пронтозил действует не сам по себе. Лечебный эффект, как это нередко бывает, оказывает продукт его распада в организме — известный еще с 1908 года сульфаниламид h3N—C6h5—SO2—Nh3. Его назвали белым стрептоцидом. С тех пор было синтезировано более 20 тыс. производных сульфаниламида, из которых в медицине используется лишь несколько десятков. В числе самых известных — стрептоцид, норсульфазол, сульфадимезин, этазол, сульфадиметоксин, фталазол, сульгин, бисептол; они отличаются строением радикала R в общей формуле сульфаниламидов (в ряде случаев замещается также один из атомов водорода в аминогруппе).
Исключительную роль в лечении многих инфекций играют антибиотики, первый из которых был случайно открыт в 1928 году. Но синтетические лекарственные средства позволяют бороться не только с бактериальными инфекциями. После открытия транквилизирующего (нейролептического) действия элениума появились десятки близких по структуре соединений, составивших большую группу транквилизаторов (нозепам, лоразепам, феназепам, тетразепам и др.).
Во многом благодаря лекарственным средствам средняя продолжительность жизни в промышленно развитых странах за последнее столетие удвоилась. Так, в Германии смертность от пневмонии, которая в 1936 году составляла 165 на 100 тысяч населения, снизилась к 1985 году в результате применения сульфаниламидных препаратов в десять раз, смертность от туберкулеза с 1930 по 1985 год уменьшилась благодаря антитуберкулезным препаратам в сто раз. В США только за период с 1965 по 1996 год удалось снизить смертность от ревматизма, атеросклероза, язвы желудка и двенадцатиперстной кишки в четыре — шесть раз.
Трудности поиска
Между химическим строением лекарственного средства и его биологическим действием нет однозначной связи. Иногда малейшие изменения структуры молекулы приводят к полному исчезновению или сильному изменению биологической активности. И наоборот, нередко почти одинаковая активность наблюдается у веществ совершенно разной химической природы. Например, если в молекуле морфина — анальгетика и наркотика заменить атом водорода в одной из гидроксильных групп на метильную группу СН3, то получится сравнительно безвредное вещество кодеин. А если оба атома водорода в гидроксильных группах заменить на две ацетильные группы СН3СО, получится молекула сильнейшего наркотика героина.

Природный алкалоид кокаин раньше применяли для местного обезболивания. Однако кокаин обладает вредным побочным действием, поэтому в медицинской практике его давно заменили синтетическим аналогом, который назвали новокаином (то есть «новым кокаином»). Эти молекулы совершенно различны по своей структуре.

Новый фармацевтический препарат получается лишь в одном случае из 25 тысяч — если действовать методом проб и ошибок. Но есть и иной принцип, который может привести к цели быстрее. Это целенаправленный синтез, включающий и накопленные за много десятилетий знания, и собственный опыт, и интуицию исследователя. Опытный специалист, взглянув на структурную формулу, с высокой достоверностью скажет, какого действия следует ожидать от этого соединения — сосудорасширяющего или, скажем, обезболивающего. Известно, какие группы и радикалы усиливают эффект, какие — ослабляют. И, тем не менее, введение в практику каждого нового фармакологического препарата требует огромных усилий множества исследователей, химиков, биологов, врачей, фармакологов; поиском новых лекарственных средств занимаются в крупнейших научных центрах во всем мире. Потому-то новые лекарства зачастую так дороги.
Частная, но важная задача
В сознании обычного человека (не химика) слово «иод» ассоциируется с пузырьком, который стоит в аптечке. Напомним, что в химических текстах принято писать «иод», а в бытовых и медицинских — «йод». На самом деле в пузырьке находится не иод, а иодная настойка — 5-процентный раствор иода в смеси спирта и воды (в настойку добавляют также иодид калия; он образует с иодом хорошо растворимый трииодид KI3). Чистый иод — твердый, напоминает с виду графит, только имеет очень специфический запах. Вот как описал иод французский химик Бернар Куртуа, который в 1811 году впервые получил его из золы морских водорослей: «Новое вещество осаждается в виде черного порошка, превращающегося при нагревании в пары великолепного фиолетового цвета. Эти пары конденсируются в форме блестящих кристаллических пластинок, имеющих блеск... Удивительная окраска паров нового вещества позволяет отличить его от всех доныне известных веществ...». По окраске паров иод и получил свое название: от греч. iodes — фиолетовый. Куртуа наблюдал еще одно необычное явление: твердый иод при нагревании не плавился, а сразу превращался в пар; такой процесс называется возгонкой. Но если кристаллы иода нагревать в пробирке быстро, они при температуре 113°C расплавятся, и на дне образуется черно-фиолетовая жидкость.
Как правило, в биохимических процессах участвуют только «легкие» элементы, находящиеся в первой трети периодической таблицы. Иод — чуть ли не единственное исключение из этого правила. В человеке содержится от 20 до 50 мг иода, значительная часть которого сконцентрирована в щитовидной железе. Щитовидная железа выделяет в кровь гормоны, оказывающие очень разностороннее влияние на организм. Два из них содержат иод — это тиреоидные гормоны (от греческого thyreoeides — щитовидный): тироксин (Т4) и трииодтиронин (Т3), молекула которого содержит на один атом иода меньше. С их помощью железа регулирует развитие и рост как отдельных органов, так и всего организма в целом, настраивает скорости обменных процессов. Процессы образования и гидролиза тиреоглобулина в щитовидной железе происходят непрерывно. В плазме крови оба гормона, Т4 и Т3, связываются с белками-переносчиками. Связь «белок — трииодтиронин» более слабая, и этот гормон легче достигает тканей, что объясняет его более высокую активность. В настоящее время трииодтиронин получают синтетически, причем по строению и действию он ничем не отличается от природного. А раньше использовали препарат тиреоидин, который делали из щитовидных желез крупного рогатого скота.

Оба тиреоидных гормона, Т3 и Т4, ускоряют реакции во всех клетках органов и тканей тела, в том числе увеличивают основной обмен, потребление кислорода, способствуют расщеплению глюкозы и жиров, повышают активность ферментов, стимулируют синтез белка, рост и дифференцировку тканей, влияют на состояние нервной и сердечно-сосудистой систем, печени, почек, других органов — в организме не так уж много гормонов, обладающих таким широким спектром действия! Более того, тироксин усиливает действие других гормонов — инсулина, адреналина, глюкокортикоидов. Поэтому поддерживать постоянный уровень Т3 и Т4 в организме жизненно важно.
Для профилактики гипотиреоза проводят мероприятия по дополнительному введению иода в рацион населения. Самый распространенный метод — иодирование поваренной соли. Обычно в нее добавляют иодид калия — примерно 25 мг на 1 кг. Однако KI во влажном теплом воздухе легко окисляется до иода, который улетучивается. Именно этим объясняется малый срок хранения такой соли — всего шесть месяцев. Поэтому в последнее время иодид калия заменяют иодатом KIO3. Кстати, это вовсе не тривиальная задача для технологов — равномерно распределить очень малое количество иода в большом объеме соли.
Помимо поваренной соли иод добавляют в витаминные смеси. Есть и такая пищевая добавка, как иодказеин. Это органическое соединение — иодированный молочный белок. Его уникальность в том, что при недостатке иода печень вырабатывает ферменты, которые расщепляют молекулы иодказеина, и высвобожденный иод всасывается в кишечнике. Если же иода в организме достаточно, то эти ферменты не вырабатываются и иод выводится из организма вместе с белком, таким образом, опасность передозировки исключается. Помимо прочего, иодказеин не распадается при высокой температуре, поэтому его можно использовать для выпечки хлеба. Для обогащения тонны хлеба иодказеином достаточно всего лишь пяти граммов белка. Суточная норма иода содержится в 250 г такого хлеба для взрослого и 100 г для ребенка.
Иодированные продукты не нужны тем, кто потребляет достаточно иода с пищей и водой. Потребность в иоде для взрослого человека мало зависит от пола и возраста и составляет примерно 150 мкг (0,15 мг) в сутки (однако она возрастает при беременности, усиленном росте, охлаждении). В большинстве пищевых продуктов иода очень мало. А вот рыба, особенно морская, богата иодом: в сельди и горбуше его 40–50 мкг, в треске, минтае и хеке — до 160 (в расчете на 100 г сухого продукта). Намного больше иода в печени трески — до 800 мкг, но особенно много его в бурых морских водорослях — «морской капусте», она же ламинария: до 500 мг! В нашей стране ламинария растет в Белом, Баренцевом и Охотском морях.
Кое-что про антибиотики
Все знают, что в названии «витамин С» буква С читается как русская «ц». Видимо, по аналогии название некогда распространенного антибиотика грамицидина С также произносят «грамицидин це». Однако это неверно: буква С в этом названии должна произноситься как «эс», от слова «советский» (можно встретить и написание «грамицидин S».) История появления этого лекарственного средства, как и многих других антибиотиков, интересна и драматична.
Когда говорят «антибиотик», чаще всего вспоминают пенициллин. Его открытие в середине ХХ века знаменовало собой новую эпоху в борьбе с болезнетворными микроорганизмами. Однако мало кто знает, что еще в начале 70-х годов XIX века врач и публицист Вячеслав Авксентьевич Манасеин и дерматолог Алексей Герасимович Полотебнов установили антибактериальные и лечебные свойства зеленой плесени. Но несовершенство химических методов не позволило в то время выделить из плесени действующее начало. В 1928 году шотландский бактериолог и биохимик Александер Флеминг (он приобрел известность еще в 1922 году благодаря открытию фермента лизоцима, см. «Химию и жизнь», 2011, № 1) заметил, что оставленная им на несколько дней культура стафилококковых бактерий покрылась плесенью. Вместо того чтобы выбросить испорченный препарат, Флеминг начал внимательно его разглядывать: он заметил, что вокруг каждого пятнышка плесени располагаются чистые области, где культура бактерий исчезла. Он понял, что в этих областях присутствует какое-то вещество, выделяемое плесневыми грибами, которое обладает сильным антибактериальным действием.
Так Флеминг открыл пенициллин. Это название происходит от рода грибов Penicillum (их около 250 видов). Флеминг использовал активный раствор пенициллина для лечения ран, но выделить действующее начало в чистом виде ему тогда не удалось: антибиотик быстро терял свои свойства при любых попытках его выделения и очистки. Справедливости ради следует сказать, что в 1985 году в архивах Лионского университета была найдена диссертация рано скончавшегося студента-медика Эрнста Августина Дюшена, в которой за сорок лет до Флеминга подробно охарактеризован открытый автором препарат из плесени Penicillium notatum, активный против многих патогенных бактерий.
Чистый препарат получил лишь десятилетие спустя английский биохимик Эрнст Борис Чейн, немец по происхождению, эмигрировавший из Германии в 1933 году. Он применил необычную для того времени методику сублимационной сушки: водный раствор препарата был заморожен до –40°C и при этой температуре из него в вакууме испарился лед. Полученные таким способом кристаллы пенициллина оказались стойкими и сохраняли свое действие в течение длительного времени.
Исследовал терапевтические свойства очищенного пенициллина и впервые применил его в лечебных целях английский патолог австралийского происхождения Говард Уолтер Флори. Ученые, открывшие и выделившие пенициллин в чистом виде, приобрели всемирную известность: Флеминг и Флори были удостоены звания пэра Британии, стали членами научных обществ и академий разных стран, а Флори был также награжден золотой медалью имени М. В. Ломоносова АН СССР. Флеминга даже избрали почетным вождем племени кайова в Северной Америке. В 1945 году Флеминг, Чейн и Флори получили Нобелевскую премию по физиологии и медицине.
В СССР исследования микробиолога Зинаиды Виссарионовны Ермольевой (в будущем — академика АМН) увенчались в 1942 году выделением пенициллина из плесени Penicillum crustorum. После войны по разработанному Ермольевой методу было организовано производство пенициллина на заводах в разных городах страны. Ермольева также первой получила отечественный стрептомицин (в 1947 году), интерферон и некоторые другие препараты.
В годы войны в работу включился американский микробиолог Зельман Ваксман. С помощью разработанных им методов он предпринял поиск микроорганизмов, вырабатывающих антибиотики (именно он ввел в употребление термин «антибиотик», от греческого слова bios — жизнь и приставки anti, означающей «противодействие»). В 1943 году он выделил из актиномицетов вида Streptomyces griseus новый антибиотик стрептомицин, который обладал широким спектром антимикробного действия. Этот препарат оказался весьма эффективным в отношении микобактерий туберкулеза, а также большинства грамотрицательных и некоторых грамположительных микроорганизмов. Стрептомицином лечили бруцеллез, чуму, другие тяжелые болезни, против которых до этого не существовало специфических средств терапии. Особенно впечатляющим было действие стрептомицина на больных туберкулезным менингитом, который ранее в 100% случаев заканчивался смертью больного в течение 20 дней.
В 1942 году из культуры бактерий, обитающих на огородных почвах Подмосковья, Г. Ф. Гаузе и М. Г. Бражниковой был выделен первый оригинальный отечественный антибиотик, который назвали грамицидином С. Биохимики А. Н. Белозерский (будущий академик, вице-президент Академии наук) и Т. С. Пасхина показали, что грамицидин С — белок. Чтобы установить его строение, необходимо было серьезное химическое исследование. В рамках тогдашнего сотрудничества союзников Минздрав СССР в 1944 году передал образец нового антибиотика в дружественную Великобританию, в Листеровский медицинский институт (Лондон). Там им занялся известный биохимик Ричард Синг. Вместе с группой коллег из города Лидса Синг выяснил, что грамицидин С — весьма необычный белок: его молекула не линейная, а циклическая. Оказалось также, что это очень простой белок, так как он содержит всего пять различных аминокислот, причем каждая из них повторяется в цикле дважды (для сравнения: яичный альбумин, основной компонент яичного белка, содержит 20 разных аминокислот, а его молекулярная масса в десятки раз больше, чем у грамицидина). Среди тех, кто занимался анализом кристаллической структуры грамицидина С, была Маргарет Тэтчер, будущий премьер-министр Великобритании, незадолго до этого защитившая диссертацию по химии.
Поскольку микроорганизмы вырабатывают устойчивость к антибиотикам, приходится постоянно изыскивать все новые и новые препараты, а также модифицировать их или полностью синтезировать (так называемые полусинтетические и синтетические антибиотики). В настоящее время описано более шести тысяч только природных антибиотиков различного происхождения (из бактерий, грибов и актиномицетов). Однако широко применяется только сотая их часть. Кроме них, известно более 100 тысяч (!) полусинтетических антибиотиков, однако лишь немногие из них обладают всем комплексом нужных свойств. При определении их эффективности учитывают не только антимикробную активность, но и скорость развития резистентности к ним микроорганизмов, степень проникновения действующего вещества в очаги поражения, возможность создания и поддержания в течение необходимого времени терапевтических, но безопасных концентраций в тканях больного и т. д.
Большинство антибиотиков получают микробиологическим синтезом с помощью специально разработанных питательных сред. Основные их производители — грибы актиномицеты, плесневые грибы и бактерии. Природные антибиотики, в том числе бензилпенициллин, цефалоспорин, рифамицин, используют главным образом для получения полусинтетических производных. Чисто синтетических антибиотиков немного. К ним относится широко известный левомицетин. По своему строению антибиотики принадлежат к самым разным классам химических соединений: среди них можно найти аминосахара, антрахиноны, гликозиды, лактоны, феназины, пиперазины, хиноны, пиридины, терпеноиды... Неудивительно, что антибиотиков известно так много. Вероятно, в будущем новые антибиотики с заранее заданными свойствами станут создавать в основном методами генной инженерии.
elementy.ru


















